近年來,研究發現一些原本被認為是老年群體特有的神經退行性疾病,如今越來越多的在年輕人身上發現。
01、認識神經退行性疾病
神經退行性疾病是一類影響神經系統功能的慢性疾病,包括阿爾茨海默病(AD)、帕金森病(PD)等。這些疾病往往伴隨著神經元死亡、突觸功能紊亂和神經網絡損傷,進而導致記憶力、思考和學習能力喪失,或者造成身體功能缺陷,給患者的生活和健康帶來巨大影響。
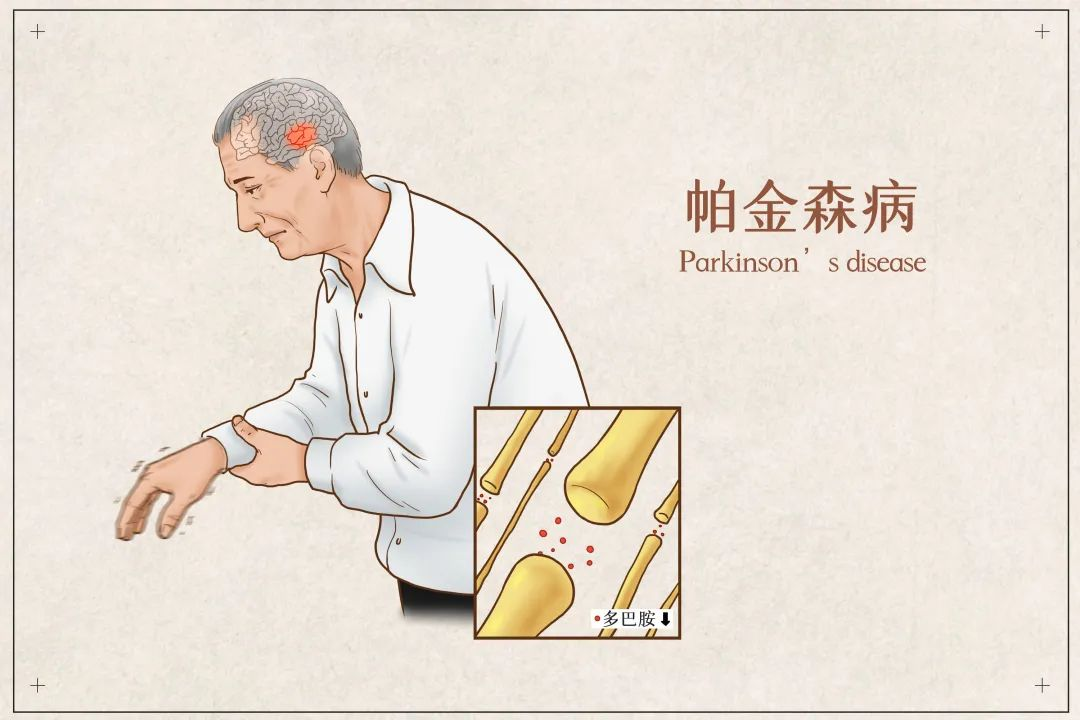
帕金森病是僅次于阿爾茨海默病的第二常見的神經退行性疾病,嚴重影響患者的日常生活,致殘率和死亡率較高。在我國,帕金森病患病人數接近300萬,預計到2030年會達到500萬人。
帕金森病的主要癥狀
運動功能喪失
慢:動作遲緩,日常的動作完成變得緩慢
抖:肢體末端難以維持固定靜止姿勢,出現不自覺抖動
僵:肌肉緊張,難以改變運動狀態
非運動癥狀
情緒抑郁、嗅覺減退、睡眠異動(容易說夢話、拳打腳踢)、認知功能下降等。
帕金森病的預防
1.避免接觸毒品和某些化學物質,如除草劑和化工原料。
2.喝咖啡和飲茶可以降低患帕金森病的風險。
3.適度的有氧運動對預防帕金森病有良好效果。
02、多巴胺與帕金森病
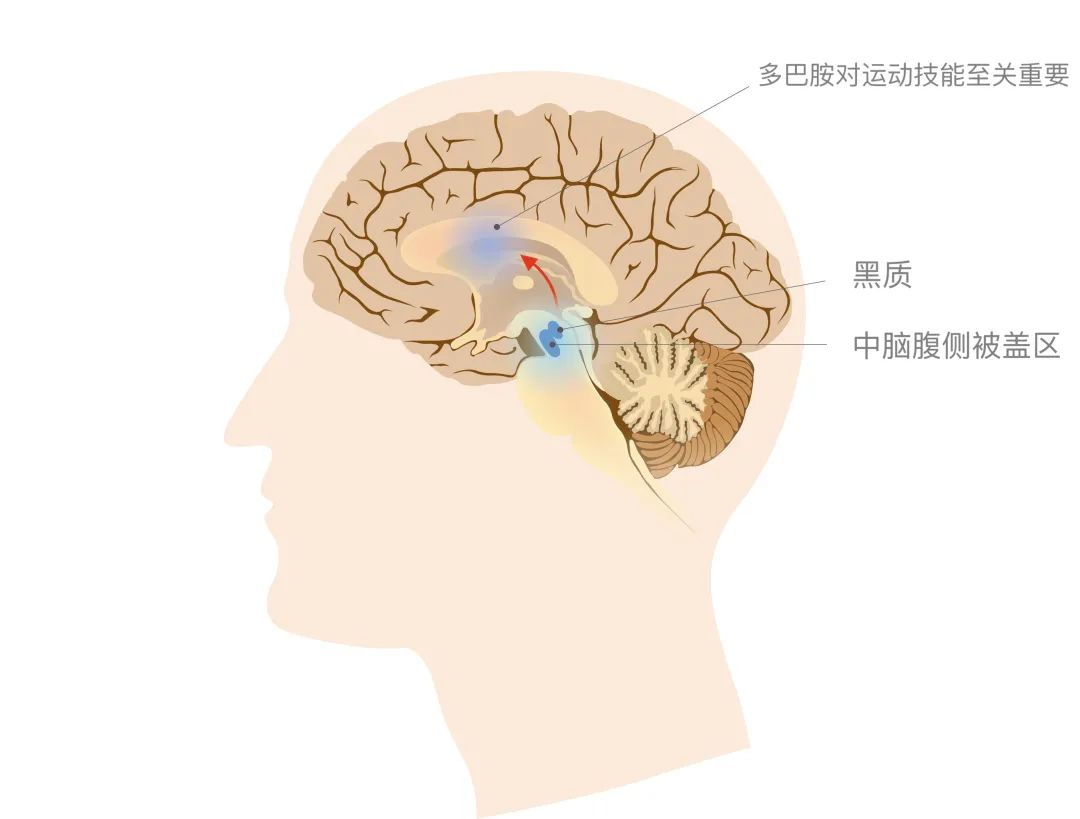
多巴胺大家應該不陌生,它除了能調節情緒,讓我們感到快樂,還具有控制運動和認知執行功能的作用。多巴胺主要產生于大腦基底核中的黑質和腹側被蓋區,黑質位于中腦被蓋和大腦腳底之間,呈半月形,黑質致密部(SNpc)的神經元含有黑色素,因此在腦切片中,這些神經元呈現黑色。黑質產生的多巴胺會通過黑質紋狀體通路(Nigrostriatalpathway)到達紋狀體,控制身體的運動動作。
圖源:攝圖網
既往研究發現,病理性α-突觸核蛋白是帕金森病的關鍵致病蛋白。在正常情況下,α-突觸核蛋白以單體形式存在,但在病理條件下,它會發生錯誤折疊并聚集在一起,破壞神經元正常功能,致使神經元死亡。它還會像“種子”一樣播散,入侵鄰近的正常神經元,誘導更多腦區α-突觸核蛋白聚集和神經元死亡,當致病蛋白傳播到中腦黑質區域時,可導致多巴胺能神經元死亡,腦內多巴胺水平下降,從而出現動作遲緩、靜止性震顫、肌強直等運動癥狀;當傳播到大腦皮層時,就會出現記憶力下降等認知障礙癥狀。
圖源:攝圖網
目前的治療方案可以采用服用補充多巴胺的藥物或腦深部刺激療法緩解運動障礙,但這些治療方案僅在短期內發揮作用,且存在副作用,不能延緩病程。
03、從0到1:帕金森病的新靶點發現
今年2月,復旦大學附屬華山醫院郁金泰團隊在Science雜志發表了帕金森病治療的新突破。研究團隊通過5年的臨床和基礎研究,在全球首次發現了帕金森病全新治療靶點FAM171A2。
FAM171A2是一種神經元細胞膜蛋白,它在神經元細胞膜上起到了“智能識別門”的作用,可以選擇性的結合病理性α-突觸核蛋白,并攜帶其進入到神經元中,誘導神經元內單體形式的α-突觸核蛋白發生錯誤折疊,造成神經元死亡和其在神經元間的傳播。
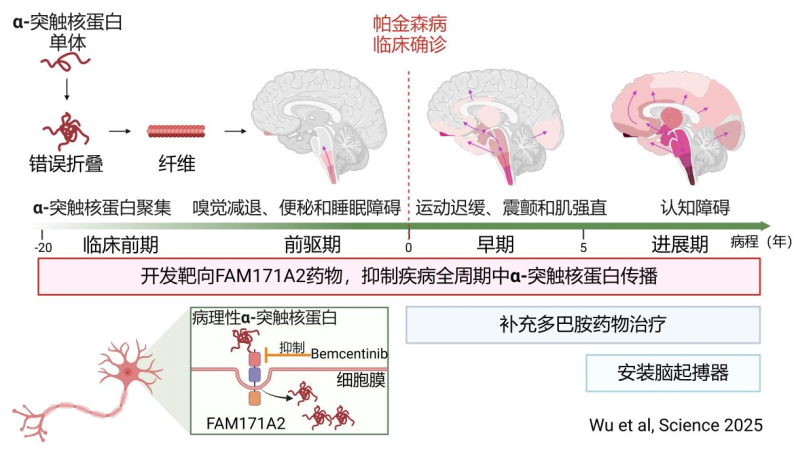
帕金森病病程進展機制及干預手段
圖源:復旦大學附屬華山醫院郁金泰團隊提供
隨后,研究團隊通過轉基因動物證實,敲除小鼠神經元上FAM171A2,可以有效控制小鼠帕金森樣癥狀的進展。基于這一發現,研究團隊利用人工智能的蛋白結構預測和虛擬篩選技術,從7000余種小分子化合物中成功找到了一種小分子可有效抑制FAM171A2蛋白和病理性α-突觸核蛋白結合,并抑制多巴胺能神經元對該致病蛋白纖維的攝取。這一小分子成為了候選的潛在治療藥物,為帕金森病治療提供了新思路。
接下來,研究團隊將全面、系統地開展尋找治療帕金森病的小分子藥物、抗體以及基因治療手段的臨床前研發工作,并進一步將相關成果推向臨床試驗和臨床應用,有望建立全球首個能夠有效阻斷帕金森病進展的創新性治療手段。
本文內容整理自第233期上海科普大講壇《追蹤FAM171A2:帕金森病治療新靶點》。
內容整理&編輯:rain
題圖圖源:攝圖網